El hígado graso agudo del embarazo (AFLP, por sus siglas en inglés) es una condición rara pero potencialmente fatal caracterizada por insuficiencia hepática. Por lo general, ocurre en el tercer trimestre del embarazo. Debido a las diferentes poblaciones de estudio, la incidencia informada varía de 1 en 7000 a 1 en 20 000 embarazos. La gravedad de este trastorno queda demostrada por datos recientes del Grupo de Estudio de Insuficiencia Hepática Aguda de EE. UU., Que muestran que la AFLP es la causa más común de insuficiencia hepática aguda durante el embarazo, más común que las causas inducidas por fármacos y la hepatitis.

Aunque AFLP comparte algunas características clínicas y de laboratorio similares con otras complicaciones médicas obstétricas, como hemólisis, enzimas hepáticas elevadas y síndrome de recuento bajo de plaquetas (HELLP), las características específicas pueden permitir el diagnóstico. El tratamiento de esta grave enfermedad requiere un reconocimiento rápido con una estrecha vigilancia clínica después del parto. En este artículo, destacaremos estas consideraciones de manejo clínico y brindaremos recomendaciones para facilitar la atención en mujeres con AFLP.
Patogénesis. La comprensión contemporánea de AFLP se estableció con el descubrimiento del síndrome de Reye en niños durante la década de 1960, donde se descubrió que las deficiencias en las enzimas mitocondriales eran responsables de los trastornos de oxidación de los ácidos grasos. Ahora se entiende que las mutaciones autosómicas recesivas en genes que codifican enzimas para la vía del metabolismo de los ácidos grasos causan tanto las características clínicas como la infiltración histológica de hepatocitos grasos microvesiculares que se observa en mujeres con AFLP.
Durante el embarazo normal, la unidad fetal-placentaria metaboliza los ácidos grasos libres para el crecimiento y desarrollo fetal. Las enzimas placentarias descomponen los triglicéridos en ácidos grasos libres, que luego se transfieren al feto. Cuando existen defectos en la vía de oxidación de los ácidos grasos de la unidad fetal-placentaria, los productos (metabolitos intermedios de los ácidos grasos) se acumulan y entran en la circulación materna. Estos metabolitos intermedios y las especies reactivas de oxígeno asociadas son absorbidos por el hígado materno para causar infiltración grasa microvesicular, activar procesos inflamatorios y causar necrosis hepática celular.
El mecanismo que conduce a la acumulación de ácidos grasos y metabolitos en el compartimento materno involucra 2 procesos. Primero, la unidad fetal-placentaria comparte una mutación homocigótica o heterocigótica compuesta que da como resultado un defecto enzimático. En segundo lugar, una madre heterocigótica tiene una capacidad disminuida para lograr la oxidación de ácidos grasos al final del embarazo, lo que conduce a una incapacidad para eliminar eficazmente los metabolitos de ácidos grasos acumulados que se han transferido desde la unidad placentaria fetal deficiente.
Factores de riesgo. Los factores de riesgo más prominentes asociados con AFLP incluyen gestaciones multifetales, fetos masculinos y los trastornos de oxidación de ácidos grasos fetales antes mencionados. Aunque la mayoría de los casos se manifiestan en el tercer trimestre, los casos notificados han ocurrido en el segundo trimestre. Otros factores de riesgo incluyen la obesidad, los trastornos metabólicos subyacentes como la diabetes mellitus y los trastornos hepáticos como la colestasis intrahepática del embarazo. Aunque existe una asociación bien conocida con la preeclampsia, la causa y el efecto directos de la AFLP no están claros. Debido a la rareza de AFLP, la vigilancia clínica de la sintomatología asociada en todos los pacientes es primordial.
Presentación clínica y evaluación. Las manifestaciones de AFLP varían desde hallazgos clínicos mínimos y alteraciones de laboratorio hasta insuficiencia hepática manifiesta con encefalopatía hepática.

Los síntomas comunes se enumeran en la Tabla 1 y a menudo se encuentran en otros "imitadores" obstétricos, como el síndrome HELLP, la toxicidad por acetaminofén y la exacerbación del lupus eritematoso sistémico.
Una de estas características clínicas, náuseas y vómitos de inicio reciente en el tercer trimestre, a menudo se asocia con AFLP y amerita una evaluación adicional. El algoritmo de prueba de la Figura 1 se puede utilizar para facilitar la evaluación en mujeres que se presentan con sospecha de AFLP. Si la preocupación clínica por AFLP sigue siendo alta después de la evaluación inicial de laboratorio, se pueden obtener más pruebas de confirmación. Estas pruebas están disponibles en la mayoría de los hospitales y se enfocan en identificar disfunción hepática y hematológica, que son las características distintivas de la AFLP.
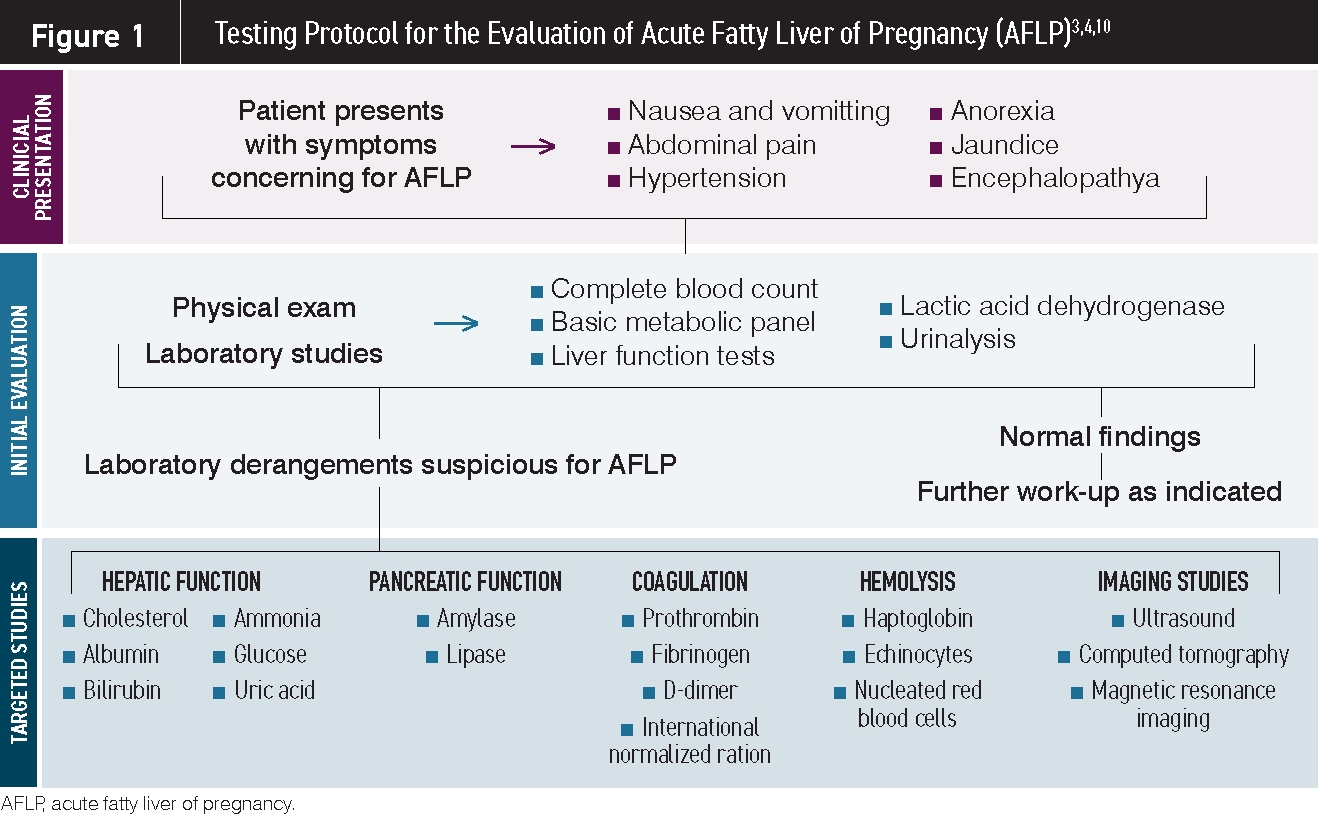
Para interpretar la batería de pruebas de laboratorio que se utilizan para diagnosticar la AFLP, es fundamental comprender los cambios fisiológicos normales del embarazo y sus alteraciones de laboratorio asociadas. Los "valores normales", como se hace referencia en un registro médico electrónico (EMR), a menudo utilizan rangos de referencia derivados de hombres y / o mujeres no embarazadas, que pueden ser profundamente anormales cuando se hace referencia a la paciente embarazada. Por ejemplo, tanto el colesterol en suero como los niveles de fibrinógeno en plasma están significativamente elevados en el tercer trimestre de un embarazo normal. Por lo tanto, si los niveles de estos analitos en el embarazo se encuentran dentro del rango de referencia de EMR, en realidad pueden ser indicativos de una anomalía significativa. No reconocer estas diferencias puede resultar en un diagnóstico perdido o una complicación no reconocida.
Clásicamente, los criterios de Swansea se utilizan para confirmar el diagnóstico de AFLP. Para cumplir con el diagnóstico de AFLP, se deben cumplir 6 de los criterios enumerados. Estos criterios están validados y son efectivos; sin embargo, utilizarlos requiere el uso de modalidades de prueba que pueden no estar fácilmente disponibles en todas las instalaciones.
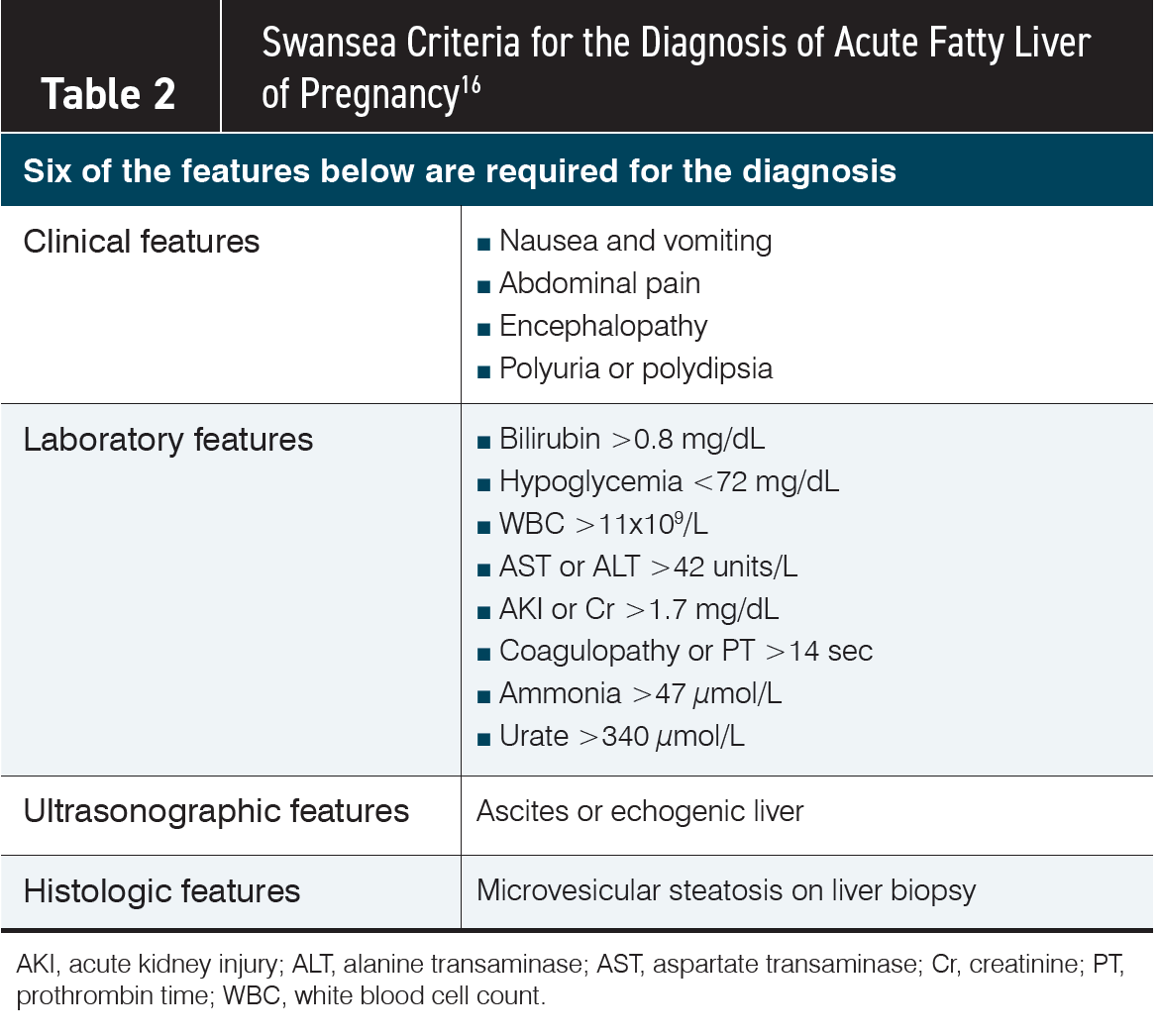
Además, algunos de estos analitos requieren un procesamiento de laboratorio específico. Por ejemplo, el muestreo de amoníaco, un analito elevado en la disfunción hepática, puede verse influenciado por el transporte de la muestra en hielo. Aunque los hallazgos ecográficos se incluyen en los criterios de Swansea, la utilidad de tales hallazgos es limitada.
Las imágenes aún pueden resultar valiosas para explorar los otros imitadores obstétricos comunes mencionados anteriormente. Por ejemplo, una ecografía del cuadrante superior derecho puede ser útil para diagnosticar un hematoma hepático en el contexto del síndrome HELLP. El uso de biopsia hepática se realizaba anteriormente para diagnosticar AFLP, pero dados los desafíos de tales pruebas en un paciente coagulopático que tiene otras características indicativas de AFLP, rara vez se utiliza en la actualidad.
Las anomalías de laboratorio asociadas con AFLP demuestran lesión multiorgánica, incluida disfunción hepática, renal y hematológica. La disfunción hepática se caracteriza por daño hepático con elevación de las transaminasas y por una función metabólica ineficaz, como lo demuestra la producción reducida de colesterol y fibrinógeno.
La insuficiencia renal, causada por lesiones tanto intrínsecas como prerrenales, se manifiesta como creatinina sérica elevada, a menudo superior a 1,0 mg / dl. Las anomalías hematológicas asociadas con frecuencia son consistentes con la coagulación intravascular diseminada, caracterizada por tiempos de coagulación prolongados, trombocitopenia, hipofibrinogenemia y productos de división de fibrina sérica elevados (dímero D). A menudo hay una hemólisis significativa, demostrada por anemia y la presencia de glóbulos rojos nucleados.
Estas características clínicas y de laboratorio pueden ser útiles para diferenciar la AFLP del síndrome de HELLP. Por ejemplo, los pacientes con AFLP tienen más probabilidades de presentar náuseas, vómitos o ictericia. Si bien la hipertensión es común a ambos diagnósticos, solo está presente en el 70% de los pacientes con AFLP y en casi todos los pacientes con síndrome HELLP. Además, la AFLP se asocia con significativamente más disfunción hepática y renal, así como coagulopatía, demostrada a través de niveles más bajos de fibrinógeno (<300 mg / dL), colesterol total más bajo (<150 mg / dL), bilirrubina total más alta (> 1.0 mg / dL) y disfunción renal más significativa (Creatinina> 1.0 mg / dL).
Gestión. El manejo clínico del paciente con AFLP se basa en los siguientes principios:
(1) reconocimiento y evaluación rápidos de la madre y el feto; (2) planificación de cuidados de apoyo, como la reversión de la coagulopatía; (3) preparación para el parto tan pronto como sea posible; y (4) atención multidisciplinaria con anestesiólogos, intensivistas, hepatólogos y pediatras.
Dada la fisiopatología subyacente de la enfermedad, se entiende que el daño hepático continuará hasta que nazca el feto. Después del parto, la recuperación materna puede ser lenta (de días a semanas) y, a menudo, requiere una atención de apoyo considerable. Cualquier mujer que presente síntomas relacionados con AFLP debe ser admitida en la unidad de trabajo de parto y parto de un hospital que tenga la capacidad de escalar la atención a un entorno de cuidados intensivos.
Una vez que la paciente ingresa, se deben iniciar una serie de medidas simultáneas en su cuidado, comenzando con una estrecha vigilancia materna y fetal. Se colocan dos catéteres intravenosos de gran calibre para la reanimación materna. Para las mujeres en las que se está considerando un diagnóstico de preeclampsia, se inicia la infusión de sulfato de magnesio para la profilaxis de la eclampsia. De hecho, la preeclampsia concurrente se observa en aproximadamente el 70% de las mujeres con AFLP. Es importante destacar que la hipertensión de rango grave se trata con agentes antihipertensivos con una presión arterial objetivo de menos de 160/110 mm Hg.
La consulta con un anestesiólogo es imprescindible para la estabilización materna y en preparación para el parto. Si el paciente está encefalopático u obnubilado, la protección de las vías respiratorias es fundamental y puede requerir intubación endotraqueal. También se puede considerar la colocación de una sonda nasogástrica con la administración de antiácidos para neutralizar el contenido del estómago en pacientes con náuseas y vómitos persistentes. Finalmente, se recomienda la consulta con el equipo pediátrico por 2 razones: (1) la necesidad de reanimación neonatal dados los riesgos de compromiso fetal; y (2) evaluación neonatal de alteraciones metabólicas después del parto.
Consideraciones del parto. Aunque el parto es necesario para el tratamiento definitivo de la AFLP, el diagnóstico por sí solo no es una indicación para el parto por cesárea. De hecho, se prefiere el parto vaginal dada la propensión a la coagulopatía grave en estas pacientes. Si se persigue el parto vaginal, se deben evitar los traumatismos vaginales, como la episiotomía. Sin embargo, la tasa de partos por cesárea en mujeres con AFLP es en última instancia significativa, tan alta como 67%, y probablemente sea impulsada por indicaciones fetales.
En la paciente sometida a cesárea, el tratamiento de la coagulopatía y la preparación para el sangrado excesivo es fundamental. Si el estado fetal lo permite, la coagulopatía debe corregirse antes de continuar con el parto. La hipofibrinogenemia debe corregirse con productos que contengan fibrinógeno (plasma fresco congelado o crioprecipitado) con un nivel de fibrinógeno objetivo de al menos 150 mg / dL.
Asimismo, la trombocitopenia debe corregirse con la administración de plaquetas a un nivel superior a 50.000 / mL. A pesar de la reanimación preoperatoria, el riesgo de hemorragia intraoperatoria y posoperatoria sigue siendo significativo. No recomendamos el uso de una incisión de Pfannenstiel y preferimos una incisión cutánea en la línea media vertical en el momento del parto por cesárea. Este enfoque aprovecha los planos quirúrgicos avasculares naturales y permite la exploración de la parte superior del abdomen si es necesario. Hemos identificado varios casos de hematomas a nivel del músculo recto en pacientes que recibieron una incisión de Pfannenstiel en el contexto de una coagulopatía concurrente con AFLP. Se puede colocar un drenaje quirúrgico en el momento del cierre abdominal si hay supuración quirúrgica o líquido ascítico en curso dentro del abdomen; sin embargo, esta no es nuestra práctica estándar.
Analgesia y anestesia. Las decisiones relativas a la anestesia y la analgesia también se verán influidas por alteraciones metabólicas y hematológicas. Para las mujeres con coagulopatía leve y trombocitopenia (plaquetas> 70.000 / ml), la anestesia neuroaxial sigue siendo una opción razonable.

Sin embargo, puede ser necesario reevaluar los índices de laboratorio antes de retirar un catéter epidural, ya que el nadir de los estudios de coagulación y el recuento de plaquetas pueden empeorar y no recuperarse hasta varios días después del parto. En casos más graves, la anestesia endotraqueal general puede ser necesaria para la protección de las vías respiratorias de la madre, la coagulopatía profunda que prohíbe la anestesia regional o en el contexto de una descompensación fetal que requiera una cesárea urgente.
Recuperación posparto y complicaciones. Si bien el parto es el tratamiento definitivo de la AFLP, la recuperación posparto puede prolongarse y complicarse debido a las necesidades continuas de atención de apoyo. Es imperativo una estrecha vigilancia y cuidados de apoyo, ya sea en una unidad de cuidados intensivos o en una unidad de trabajo de parto y parto. Las mediciones seriadas de la función hematológica, hepática y renal deben realizarse cada 6 a 12 horas durante los primeros 1 a 2 días. La anemia es común durante este tiempo debido a hemólisis o hemorragia posparto, y con frecuencia requiere transfusión.
Además, en pacientes con disfunción renal que reciben sulfato de magnesio para la profilaxis de las convulsiones, se deben controlar los niveles séricos de magnesio para evitar la toxicidad por magnesio. Los niveles de glucosa en sangre también deben controlarse cada hora. Si los niveles caen por debajo de 60 mg / dL, la hipoglucemia debe tratarse con una infusión de glucosa al 10%.
Se debe esperar una recuperación gradual de los analitos de laboratorio dentro de una semana después del parto. La disfunción hepática generalmente comienza a mejorar de 1 a 2 días después del parto. Los niveles de transaminasas disminuyen linealmente a niveles de 100 unidades / L o menos, y pueden permanecer levemente elevados durante varias semanas.
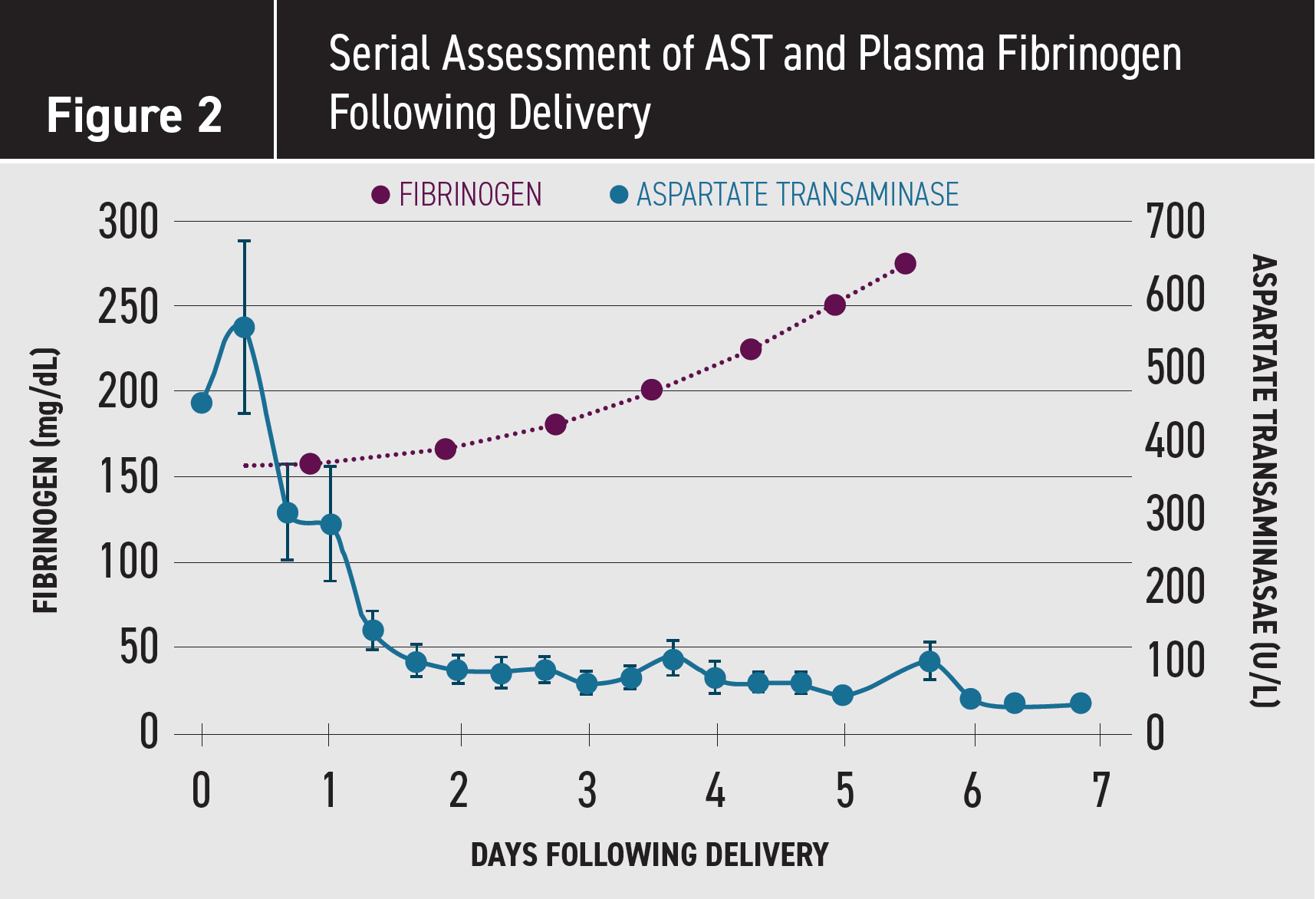
Otros marcadores de disfunción hepática, incluidos el colesterol y la bilirrubina total, comienzan a mejorar después de 3 a 4 días. La disfunción hemostática relacionada con la función hepática sintética o con la coagulopatía de consumo mejora entre 4 y 6 días después del parto, como lo indica el aumento del fibrinógeno plasmático y la disminución del dímero-D. Por el contrario, la recuperación renal medida por la creatinina sérica puede requerir de 7 a 10 días.
El curso posparto puede complicarse aún más en algunas pacientes. Hasta el 15% de las mujeres con AFLP desarrollarán pancreatitis. Esto se maneja de forma conservadora con hidratación intravenosa, analgesia y descompresión nasogástrica. También puede haber diabetes insípida transitoria y, en la mayoría de los casos, se puede ralentizar la diuresis excesiva con desmopresina.
En raras ocasiones, no se produce la recuperación hepática esperada y se produce una insuficiencia hepática persistente. Esto requiere tratamiento por parte de hepatólogos e intensivistas y puede implicar el uso de terapias avanzadas, como intercambio de plasma o sistemas de soporte vital extracorpóreo. El trasplante puede ser necesario en pacientes con insuficiencia hepática persistente profunda con hipotensión y acidosis. La necesidad de un trasplante suele ser más tardía en el curso de recuperación y lejos del parto.
Resultados maternos y perinatales. Junto con los avances en el diagnóstico y el tratamiento de la AFLP, los resultados maternos y perinatales han mejorado significativamente en las últimas 2 décadas. La mortalidad materna, que alcanzaba entre el 80% y el 90% en la década de 1980, ahora ha disminuido a menos del 10%. La mortalidad perinatal sigue siendo sustancial y ahora se registra en aproximadamente el 20% de los casos de AFLP. En una revisión reciente de más de 350 mujeres con AFLP, todas las sobrevivientes tuvieron una recuperación completa de la función hepática. A pesar de estas mejoras, la morbilidad sigue siendo significativa.
Con altas tasas de lesión renal aguda asociada, ingreso a la unidad de cuidados intensivos y transfusión de sangre y componentes, la mayoría de los casos desencadenarán un evento de morbilidad materna grave. La recurrencia de AFLP en un embarazo posterior es rara, pero las mujeres que son heterocigotas para un defecto de la enzima de oxidación de ácidos grasos tienen un mayor riesgo. Por lo tanto, se debe considerar la detección de trastornos por oxidación de ácidos grasos en mujeres con antecedentes de AFLP.

No hay comentarios:
Publicar un comentario