La diabetes mellitus gestacional (DMG) es la complicación médica más común del embarazo y su tasa ha seguido aumentando en los Estados Unidos. Actualmente, afecta aproximadamente a 1 de cada 10 o 380.000 mujeres embarazadas por año, y casi el 90% de los casos de diabetes en el embarazo representan DMG. La prevalencia de la afección se ha más que duplicado entre las mujeres no blancas, con sobrepeso y de bajos ingresos en la última década en un entorno de edad materna creciente, obesidad y vida sedentaria.
En esta revisión clínica, proporcionamos una descripción general de la epidemiología, la detección y el tratamiento clínico de la diabetes gestacional.
Impacto de la DMG en los resultados adversos del embarazo y el tratamiento para reducir el riesgo.
La DMG más que duplica el riesgo de morbilidad y mortalidad perinatal, y este riesgo aumenta progresivamente con la gravedad de la hiperglucemia y disminuye con el tratamiento, incluidos los cambios en el estilo de vida y la farmacoterapia. Para el bebé, la hiperglucemia materna puede causar hiperinsulinemia fetal, que resulta en un crecimiento fetal excesivo (macrosomía, grande para la edad gestacional), traumatismo de nacimiento, hipoglucemia neonatal, retraso en el desarrollo pulmonar e hipoxia fetal. Para la madre, la diabetes gestacional aumenta el riesgo de distocia de hombros, parto por cesárea y preeclampsia.
Históricamente, los criterios empleados para diagnosticar la diabetes gestacional se basaban en la probabilidad de desarrollar diabetes tipo 2 más adelante en la vida, en lugar de identificar a las personas con mayor riesgo de resultados perinatales adversos debido a la intolerancia a la glucosa. El estudio histórico de hiperglucemia y resultado adverso del embarazo (HAPO) ayudó a establecer criterios de diagnóstico acordados internacionalmente para la DMG en más de 25.000 embarazos. Este estudio demostró que el aumento de la hiperglucemia definida por elevaciones en los 3 valores de 75 g, Los resultados de HAPO llevaron al grupo de trabajo de la Asociación Internacional de Grupos de Estudio de la Diabetes y el Embarazo (IADPSG) a recomendar una prueba de 1 paso para la detección de DMG. Sin embargo, después de una revisión sistemática de los hallazgos, la Conferencia de Desarrollo de Consenso de los Institutos Nacionales de Salud sobre el diagnóstico de DMG encontró evidencia insuficiente de beneficio materno o perinatal para adoptar una prueba de detección y, más bien, continuó respaldando un enfoque de 2 pasos para la detección y diagnóstico.
Cuándo y cómo detectar GDM. La diabetes gestacional es un estado restringido a las mujeres embarazadas cuya intolerancia a la glucosa se descubre por primera vez durante el embarazo. La mayoría de estas mujeres tendrán niveles normales de glucosa en ayunas; por lo tanto, se requiere una prueba de glucosa para desenmascarar este estado. Históricamente, los factores de riesgo que incluyen antecedentes familiares de diabetes, antecedentes de macrosomía o muerte fetal, obesidad, hipertensión crónica y edad materna se utilizaron para evaluar a las mujeres con mayor riesgo de DMG. El problema es que más de la mitad de las mujeres con un GTT anormal carecen de factores de riesgo.
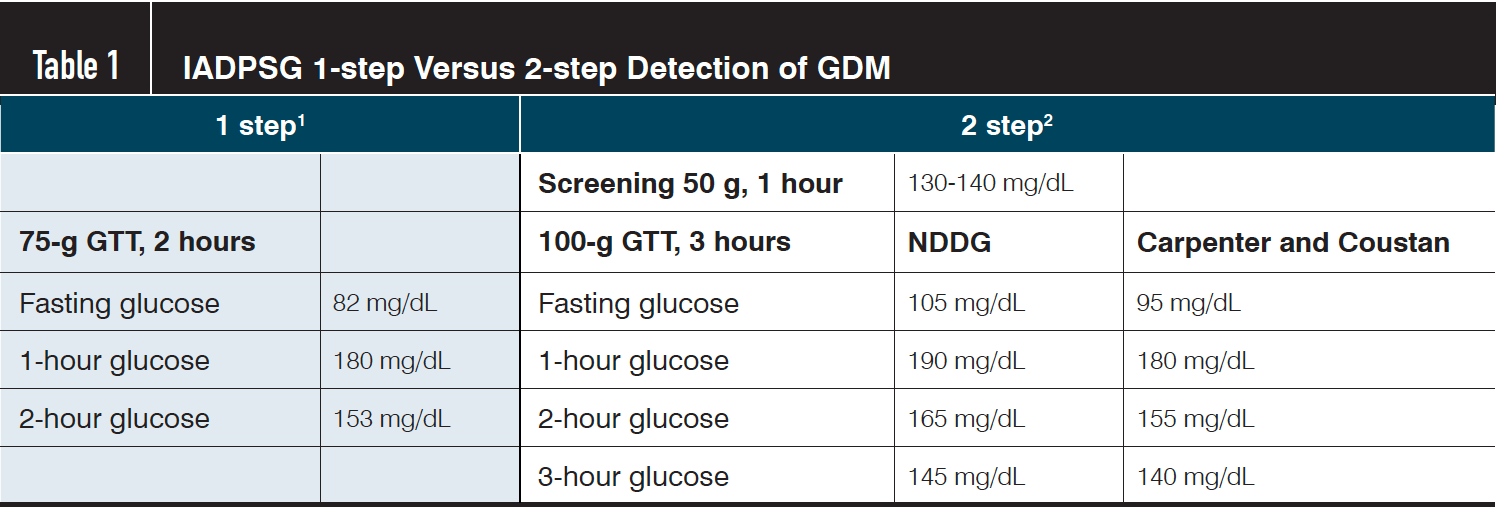
1 Se realiza un diagnóstico de 1 paso si se alcanza o se supera 1 valor.
2 Se realiza un diagnóstico de 2 pasos cuando se alcanzan o superan 2 valores cualesquiera del GTT.
El Colegio Estadounidense de Obstetras y Ginecólogos (ACOG) recomienda la detección universal para todas las mujeres embarazadas. El cribado generalmente se realiza entre las 24 y 28 semanas cuando se ha establecido el “estado diabetogénico” del embarazo. Dos estrategias de detección comúnmente utilizadas incluyen una prueba de 1 paso respaldada por IADPSG versus una prueba de 2 pasos respaldada por ACOG (Tabla 1).
Una prueba de 1 paso incluye una GTT oral de 75 g, de 2 horas en la que se puede hacer un diagnóstico de DMG cuando se alcanza o se supera un valor único.
Una prueba de 2 pasos implica una prueba de provocación de glucosa inicial de 50 g seguida de una prueba de GTT oral de 100 g de 3 horas.
La prueba inicial de 50 g de glucosa se puede realizar en ayunas o después de comer. Un valor plasmático entre 130 y 140 mg / dL se usa generalmente como umbral para realizar una GTT oral de 3 horas. Para diagnosticar la DMG según el GTT de 3 horas, el ACOG respalda los criterios del Grupo Nacional de Datos de Diabetes (NDDG) o los criterios menos estrictos de Carpenter y Coustan. Independientemente de cualquier conjunto de criterios, si 2 o más de 4 valores de GTT oral exceden los umbrales establecidos, se confirma el diagnóstico de DMG.
Los resultados de múltiples estudios han demostrado que, aunque se puede identificar un mayor número de mujeres (casi el doble) con DMG utilizando los criterios de 1 paso de la IADPSG en comparación con los criterios de 2 pasos; lo que es más importante, esto no da como resultado una disminución de los resultados neonatales adversos, incluida la macrosomía.
Para resumir el dilema actual con respecto a estas 2 estrategias de detección, la Asociación Estadounidense de Diabetes (ADA) concluye que (1) los datos son insuficientes para demostrar la superioridad de una estrategia sobre la otra; (2) decidir qué estrategia utilizar en la práctica clínica puede verse afectada por otros factores, incluido el costo-beneficio, la voluntad de cambiar la práctica y las consideraciones de costo e infraestructura; y (3) se necesita más investigación.
Este año, Hillier et al informaron los hallazgos de un gran ensayo pragmático que comparó el enfoque de un solo paso con el de 2 pasos entre casi 24,000 mujeres embarazadas. De acuerdo con los datos previos utilizando los criterios de la IADPSG, la frecuencia de una DMG fue el doble en comparación con el enfoque de 2 pasos (17% frente a 9%). Sin embargo, la frecuencia de los trastornos hipertensivos del embarazo, el parto por cesárea primaria y los lactantes grandes para la edad gestacional y el resultado perinatal combinado no fueron diferentes entre los grupos de prueba. Los hallazgos de este estudio destacan que, si bien una prueba de detección de 1 paso puede detectar más mujeres con DMG que una de 2 pasos, es posible que no haya un beneficio materno o perinatal aparente en general con este enfoque.
Finalmente, el ACOG recomienda la detección temprana en el embarazo para mujeres con antecedentes de DMG, alteración del metabolismo de la glucosa o enfermedad cardiovascular que hayan dado a luz a un bebé que pese 4000 go más, tengan sobrepeso u obesidad, tengan un familiar de primer grado con diabetes y estén miembros de grupos raciales y étnicos de alto riesgo. Un método sencillo para diagnosticar la diabetes al principio del embarazo es obtener un nivel de HbA1C. Un valor mayor o igual al 6.5% es consistente con un diagnóstico de diabetes tipo 2 independientemente del embarazo y no requiere más pruebas. Las mujeres con un nivel de HbA1C entre el 5,7% y el 6,4%, lo que es compatible con una intolerancia a la glucosa, deben someterse a un diagnóstico de GTT oral, ya que 1 de cada 4 puede desarrollar DMG más adelante. Aquellos con un nivel de HbA1C inferior al 5,7% pueden someterse a exámenes de detección de rutina entre las 24 y 28 semanas.
Tratamiento de primera línea para la diabetes gestacional: intervención en el estilo de vida. Los pilares del tratamiento de la DMG comienzan con intervenciones en el estilo de vida, que incluyen asesoramiento nutricional, cambios en la dieta y ejercicio diario, con el objetivo de disminuir la hiperglucemia posprandial (tabla 2). Los cambios en la dieta y la nutrición pueden incluir limitar los carbohidratos a menos del 40% de las calorías, aumentando el complejo en relación con los carbohidratos simples. El ejercicio diario recomendado incluye 30 minutos de ejercicio aeróbico de intensidad moderada al menos 5 días a la semana. Es de destacar que la mayoría de las mujeres con DMG pueden ser obesas, y las recomendaciones de aumento de peso gestacional del Instituto de Medicina de 2009 no hacen recomendaciones específicas con respecto a las mujeres con DMG.

Los resultados de 2 ensayos importantes durante los últimos 20 años han demostrado que las intervenciones en el estilo de vida para la diabetes gestacional brindan beneficios tanto para la madre como para el lactante. El Estudio Australiano de Intolerancia a los Carbohidratos en Mujeres Embarazadas fue un ensayo controlado aleatorio (ECA) multicéntrico de 10 años de 1000 mujeres que demostró una reducción significativa en el compuesto primario (muerte perinatal, distocia de hombros, trauma al nacer).
En el ECA de la Red de Unidades de Medicina Materno Fetal del Instituto Nacional de Salud Infantil y Desarrollo Humano de 928 mujeres con DMG leve, los investigadores no encontraron diferencias en la frecuencia del compuesto primario (muerte perinatal, hipoglucemia neonatal, nivel elevado de péptido C del cordón o trauma de nacimiento) con tratamiento versus atención estándar. Sin embargo, sí encontraron una disminución en el riesgo de sobrecrecimiento fetal, masa grasa neonatal, distocia de hombros, parto por cesárea y trastornos hipertensivos del embarazo. En conjunto, estos 2 estudios demuestran el beneficio del tratamiento de incluso una intolerancia leve a los carbohidratos durante el embarazo.
Una vez que el paciente comienza con una dieta y un plan de ejercicio adecuados, es necesaria una estrecha vigilancia de los niveles de glucosa en sangre para garantizar que se mantenga el control glucémico. Esto generalmente se logra con pacientes que realizan controles diarios de glucosa en sangre, que incluyen un nivel de ayuno y 3 mediciones posprandiales 1 o 2 horas después de cada comida. Los umbrales glucémicos objetivo de la glucosa en ayunas son menos de 95 mg / dL, glucosa posprandial 1 hora menos de 140 mg / dL y glucosa posprandial 2 horas menos de 120 mg / dL (Tabla 3).
ACOG y ADA recomiendan los mismos umbrales para DMG y diabetes pregestacional. 11Una vez que las mujeres logran y mantienen un buen control glucémico, se puede reducir la frecuencia de las pruebas. Si estos objetivos no se pueden alcanzar y la mayoría de los valores en ayunas y / o posprandiales están elevados, se recomienda la farmacoterapia.

Es de destacar que para las mujeres con diabetes pregestacional, la monitorización de la glucosa se realiza cada vez más mediante la monitorización continua de la glucosa (MCG). Actualmente, esta tecnología no se utiliza ampliamente para la diabetes gestacional, aunque los datos emergentes sugieren que la MCG puede identificar momentos específicos del día que no se identifican con el control de glucosa en sangre de rutina, como la hiperglucemia nocturna, que puede estar asociada con un mayor riesgo de efectos perinatales adversos. resultados.
Cuándo iniciar la farmacoterapia y qué medicamento usar. El desafío es que al menos 1 de cada 4 mujeres con DMG no responden a la intervención en el estilo de vida, incluida la dieta y el ejercicio, y requieren farmacoterapia para lograr la euglucemia.
No se ha establecido el umbral óptimo para iniciar la terapia farmacológica. La mayoría de los médicos inician la farmacoterapia cuando del 30% al 50% o más de los valores de punción en el dedo están por encima del rango objetivo (glucosa posprandial en ayunas y 2 horas ≥95 mg / dL y ≥120 mg / dL, respectivamente) en la última semana. Tanto el ACOG como la ADA recomiendan la insulina como tratamiento de primera línea porque no atraviesa la placenta y mejora los resultados perinatales. La Sociedad de Medicina Materno-Fetal recomienda la metformina o la insulina como opciones razonables de primera línea.
Aunque se pueden usar regímenes de insulina basados en el peso por trimestre del embarazo, para lo cual hay calculadoras en línea disponibles, un enfoque más simple para la práctica clínica es iniciar una dosis única de protamina neutra Hagedorn (NPH) de acción prolongada o insulina detemir a la hora de acostarse para tratar la hiperglucemia en ayunas. Se puede usar insulina lispro o aspart de acción más corta para atacar la hiperglucemia posprandial. En nuestra práctica, generalmente comenzamos con 12 a 20 U NPH de insulina por la mañana y 10 U NPH a la hora de acostarse. Luego, se pueden usar de 5 a 10 U de insulina de acción corta para abordar las excursiones a la hora de comer. Para un paciente para quien la hiperglucemia en ayunas es la única indicación de farmacoterapia, comenzamos con una sola inyección de insulina de acción prolongada antes de acostarse. Recomendamos un enfoque conservador para el inicio de la insulina para evitar la hipoglucemia,
Los agentes hipoglucemiantes orales, como la metformina y la gliburida, se han convertido cada vez más en una alternativa popular a la insulina inyectable durante las últimas dos décadas. Históricamente, la gliburida, una sulfonilurea, había sido un agente oral de uso frecuente para la DMG. La metformina, una biguanida, reduce tanto la glucosa basal como la posprandial, y es el agente de primera línea preferido para tratar la diabetes tipo 2 fuera del embarazo. Una opción oral puede ser preferible a las inyecciones frecuentes debido a su conveniencia, menor costo, facilidad de administración y mejor adherencia. La cobertura del seguro y el costo de la insulina han sido cada vez más problemas, especialmente para los pacientes con seguro público. En muchas áreas, esto ha restringido el formulario de insulina disponible.
Sigue existiendo una gran controversia sobre el uso de agentes orales para la diabetes gestacional. Existen preocupaciones persistentes sobre la eficacia de los agentes orales para prevenir resultados neonatales adversos en comparación con la insulina y el hecho de que los agentes orales (metformina y gliburida), a diferencia de la insulina, atraviesan la placenta. Hemos encontrado que, en la práctica, las mujeres con hiperglucemia en ayunas (> 115 mg / dl) generalmente no lograrán un control glucémico adecuado con agentes orales.
En el histórico ensayo Metformin in Gestational Diabetes (MiG), cuyos resultados se publicaron en 2008, Rowan y sus colegas asignaron al azar a 761 mujeres con DMG a insulina o metformina. Observaron que el riesgo del resultado combinado (hipoglucemia neonatal, dificultad respiratoria, trauma al nacer, parto prematuro y necesidad de fototerapia en el lactante) se observó en aproximadamente un tercio de las mujeres en ambos grupos. Es de destacar que más del 40% de las mujeres que recibieron metformina requirió insulina suplementaria para lograr un control glucémico adecuado.
En 2018, Senat y sus colegas asignaron al azar a 914 mujeres a recibir insulina o gliburida, y observaron mejoras similares en la glucemia con cada régimen. Sin embargo, la frecuencia de macrosomía e hipoglucemia neonatal fue similar entre ambos grupos. Varios metanálisis sugieren que los agentes orales, en particular la metformina, son equivalentes, si no superiores, en la prevención de resultados neonatales adversos. Sin embargo, las limitaciones importantes de los estudios incluidos son los criterios de diagnóstico poco claros y la incapacidad de ajustar el impacto de la gravedad de la hiperglucemia en los resultados del tratamiento; Poblaciones heterogéneas mal caracterizadas, a menudo de países de ingresos bajos y medianos, criterios poco claros para la insulina suplementaria y tamaño de muestra pequeño.
Si la metformina coloca a los niños expuestos y a las madres en mayor riesgo de enfermedad metabólica después del parto, aún no se ha esclarecido por completo. A diferencia de la insulina, que no atraviesa la placenta, la metformina plantea una preocupación real debido al potencial teórico para la programación del desarrollo de la disfunción metabólica en los niños expuestos en el útero. Los investigadores del ensayo MiG informaron que en un subconjunto de niños con un seguimiento de 5 a 7 años, los expuestos a la metformina tenían un índice de masa corporal (IMC, es decir, más pesado) más alto que los expuestos a la insulina. Un metaanálisis reciente afirmó que a los 2 años, los niños expuestos a metformina tenían un IMC más alto en comparación con los expuestos a insulina. Por lo tanto, abordar la seguridad a largo plazo de los agentes orales para la diabetes gestacional sigue siendo una prioridad de investigación importante.
Gestión anteparto y parto. Las mujeres con DMG bien controlada tienen un riesgo bajo de muerte fetal intrauterina y, por lo tanto, las pruebas fetales preparto de rutina generalmente no se inician para DMG de clase A1 no complicada controlada por dieta. Pero para las mujeres con un trastorno hipertensivo, muerte fetal previa o sospecha de macrosomía, se realizan pruebas fetales. Además, las mujeres en tratamiento farmacológico con insulina y / o agentes orales (clase A2) se someten al menos a pruebas fetales semanales a partir de las 32 semanas de gestación.
Con respecto al momento del parto, muchos obstetras han extrapolado el mayor riesgo de muerte fetal intrauterina en mujeres con diabetes tipo 1 y 2 a aquellas con DMG; por lo tanto, a las mujeres con DMG en tratamiento farmacológico generalmente se les recomienda que se sometan a la inducción en la semana 39. El ACOG recomienda actualmente que para las mujeres con DMG bien controlada con dieta sola (clase A1) se considere el parto a las 39 + 0 a 40 + 6 semanas. Para aquellos pacientes que reciben farmacoterapia (clase A2), se debe considerar el parto a las 39 + 0 a 39 + 6 semanas. Si el control glucémico es subóptimo, entonces se debe considerar el parto a las 37 + 0 a 38 + 6 semanas. Como guía, para las mujeres con diabetes preexistente, se ofrece un parto por cesárea programada para prevenir traumatismos en el parto a aquellas con sospecha de macrosomía (4500 go más al nacer) o antecedentes de distocia de hombros previa.
Detección posparto de diabetes tipo 2 y efecto de la diabetes gestacional en la salud futura. Las mujeres con DMG tienen un mayor riesgo de desarrollar intolerancia a la glucosa más adelante en la vida, o un riesgo aproximadamente 7 veces mayor de desarrollar diabetes tipo 2 en comparación con aquellas sin DMG. Entre las mujeres hispanas, casi dos tercios pueden desarrollar diabetes tipo 2 en 5 años después del índice de embarazo con DMG. Para el momento de la prueba posparto entre las 6 y 12 semanas después del parto, aproximadamente 1 de cada 3 mujeres recibirán un diagnóstico de diabetes tipo 2 manifiesta, glucosa en ayunas alterada o tolerancia a la glucosa alterada. El riesgo de diabetes tipo 2 posterior aumenta cuando la diabetes se diagnostica en una etapa temprana del embarazo o cuando los niveles de glucosa en ayunas de la madre son más altos. Algunas de estas mujeres pueden representar casos de diabetes tipo 2 preexistente no identificada.

Tanto la ADA como la ACOG recomiendan la prueba de glucosa posparto utilizando glucosa plasmática en ayunas o una GTT oral de 75 g durante 2 horas entre 4 y 12 semanas después del parto para un embarazo complicado por DMG (tabla 4) . Aún no se ha establecido la frecuencia de las pruebas, la ADA apoya la repetición de las pruebas cada 3 años para las mujeres con DMG previa y resultados normales de detección posparto. El problema es que solo alrededor de 1 de cada 5 mujeres con DMG se someten a exámenes de detección posparto y se necesitan estrategias innovadoras para aumentar su aceptación.
Las mujeres también deben recibir asesoramiento sobre el riesgo de recurrencia de la diabetes gestacional en un embarazo posterior, que puede llegar hasta el 40%. Las formas importantes de disminuir el riesgo de diabetes tipo 2 incluyen la lactancia materna, los cambios en el estilo de vida y la farmacoterapia con metformina. La DMG puede estar asociada con un mayor riesgo de obesidad infantil y disfunción metabólica posterior en el lactante. Aún no se sabe hasta qué punto la programación fetal de la función metabólica en la DMG tiene un efecto intergeneracional que puede modificarse con el tratamiento.
Conclusiones.
- La DMG es una de las complicaciones médicas más comunes del embarazo y su frecuencia casi se ha duplicado en la última década en un ambiente obesogénico. La DMG duplica el riesgo de morbilidad y mortalidad perinatal.
- Todas las mujeres embarazadas deben someterse a pruebas de detección de diabetes gestacional y, en la actualidad, se utiliza con mayor frecuencia un enfoque de detección de dos pasos.
- El tratamiento de primera línea incluye intervenciones en el estilo de vida, pero casi 1 de cada 4 mujeres requerirá farmacoterapia. La insulina es generalmente la farmacoterapia de primera línea preferida, pero se necesitan más investigaciones con respecto a la eficacia y seguridad de los agentes orales, en particular la metformina.
- Las pruebas prenatales generalmente se inician a fines del tercer trimestre, y el parto a menudo se recomienda para la semana 39.
- Todas las mujeres con DMG deben someterse a pruebas de detección de intolerancia a la glucosa y diabetes tipo 2 en el período posparto con un seguimiento basado en los resultados de GTT oral de 75 g.

No hay comentarios:
Publicar un comentario