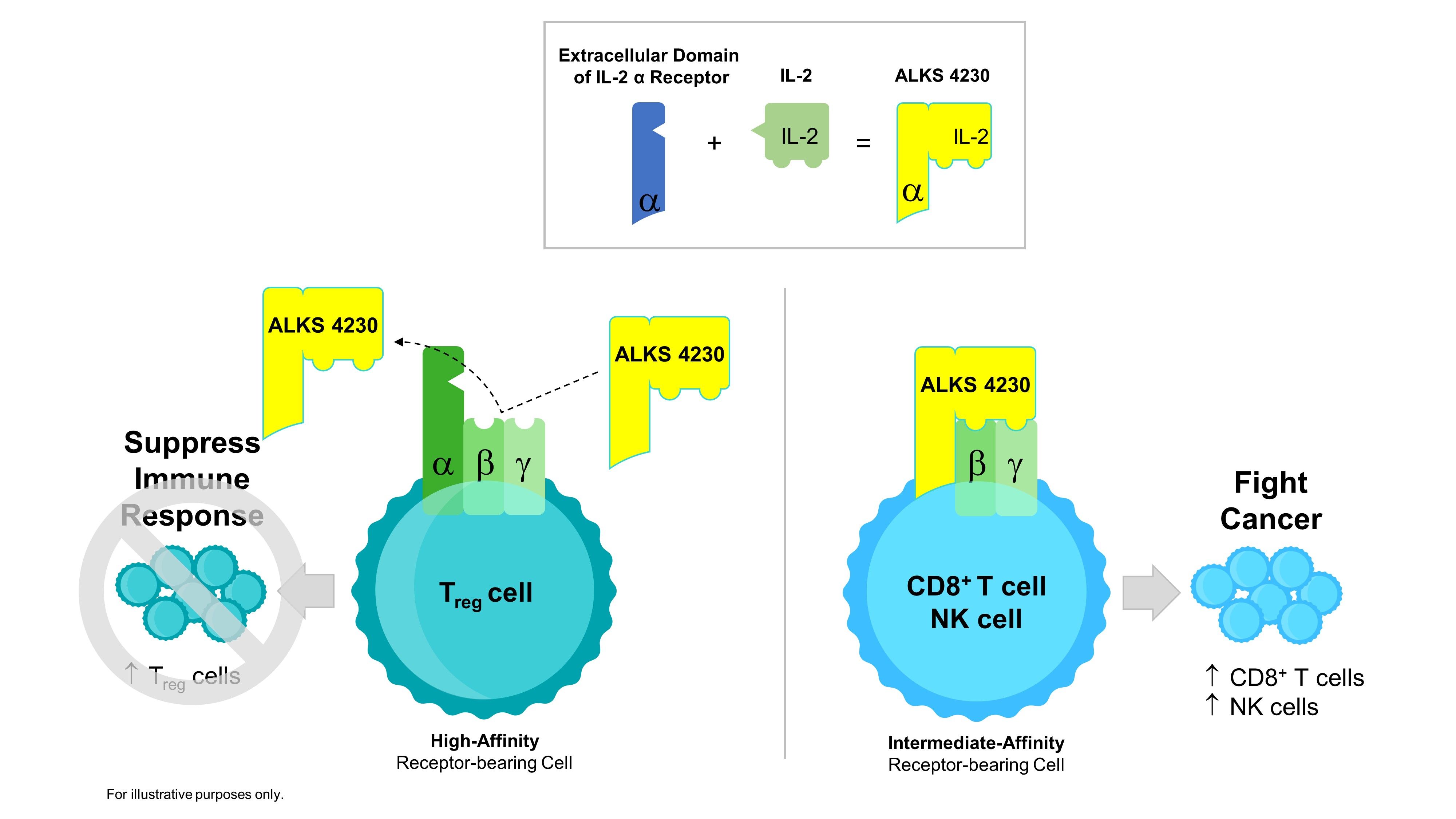
Las pacientes con cáncer de ovario muy pretratadas que recibieron una terapia combinada de una nueva citocina interleucina-2 (IL-2) más pembrolizumab lograron un perfil de seguridad aceptable. El estudio también encontró evidencia limitada de reducción del tumor y estabilización de la enfermedad en algunos pacientes.
El ensayo ARTISTRY-1 está patrocinado por Alkermes plc (Dublín, Irlanda), fabricante de la citocina ALKS 4230, que se administra por vía intravenosa como monoterapia y en combinación con pembrolizumab. Existe una gran necesidad insatisfecha en el espacio del cáncer ginecológico, especialmente para el cáncer de ovario resistente al platino. Las pacientes con cáncer de ovario resistente al platino y refractario normalmente no les va bien. Se necesitan desesperadamente nuevos agentes y vías terapéuticas.
La fase de combinación de ARTISTRY-1, que comprende un subgrupo de 15 pacientes con cáncer de ovario, se inició en el Instituto de Cáncer Karmanos hace aproximadamente 2 años. Los pacientes tienen entre 48 y 83 años, con una edad promedio de 74. Antes del estudio, estas pacientes con cáncer de ovario habían recibido una mediana de cinco regímenes, que iban de dos a 11, y todos habían sido tratados previamente con terapia basada en platino.
Aunque los inhibidores de puntos de control están aprobados para tratar varios tipos de cáncer, hasta la fecha tienen un éxito limitado para el cáncer de ovario. Solo hay una tasa de respuesta del 10% al 15% en pacientes aptos para la terapia de inmunoncología (IO) prototípica El objetivo es mejorar estos resultados.
Luego, durante el período de estudio, cada paciente participó en uno o más ciclos de terapia de 21 días, con una duración media del tratamiento de aproximadamente 7 semanas. Cada ciclo consistió en ALKS 4230 (3 µg / kg) los días 1 a 5 y pembrolizumab (200 mg) solo el día 1.
Los cambios en el microambiente tumoral (TME) se calcularon utilizando biopsias iniciales y durante el tratamiento. Entre 13 pacientes evaluables (al menos una evaluación posterior al tratamiento), 9 pacientes lograron el control de la enfermedad o la enfermedad estable en la primera exploración y los otros 4 experimentaron progresión de la enfermedad. Cinco pacientes experimentaron una reducción del tumor durante más de 20 semanas, incluidos 3 pacientes que experimentaron una respuesta objetiva: 1 respuesta completa (desaparición completa del cáncer), 1 respuesta parcial y 1 respuesta parcial no confirmada.
Tres de estas pacientes eran resistentes al platino y negativos para mutaciones BRCA. Inesperadamente, la paciente con la respuesta completa recibió un tratamiento previo intenso y ha participado en el ensayo durante más de 1 año. La calidad y la cantidad de vida son importantes en las pacientes con cáncer de ovario, como con todas las enfermedades, y esta paciente ha visto ambas, a pesar de estar en un régimen tan intensivo.
Para el cáncer de ovario, las respuestas del estudio serían raras solo con los inhibidores de los puntos de control. De hecho, una respuesta de inhibidor de un solo punto de control sería anecdótica.
Los eventos adversos relacionados con el tratamiento a las dosis probadas generalmente han sido transitorios y manejables, siendo la mayoría de gravedad de grado 1 o grado 2. La citoquina no mostró ninguna toxicidad aditiva a la ya establecida con pembrolizumab solo.
La forma en que está diseñado ALKS 4230 ayuda a modular el entorno inmunológico y las propias células inmunitarias para hacer que el inhibidor del punto de control prototípico funcione mejor.

No hay comentarios:
Publicar un comentario