El riesgo de tromboembolismo venoso es particularmente alto durante el período posparto y especialmente después de un parto por cesárea. El tromboembolismo venoso (TEV) es una de las principales causas de morbilidad y mortalidad materna. La incidencia estimada de TEV durante el embarazo y el posparto es de 1 a 2 por 1000 partos. El riesgo de TEV es particularmente alto durante el período posparto y especialmente después de un parto por cesárea.
Existe una variación considerable en el enfoque de la profilaxis de la TEV durante el embarazo, incluso después de un parto por cesárea. Las guías recientes de varias organizaciones profesionales brindan recomendaciones contradictorias basadas en evidencia de bajo grado, principalmente de datos de observación.
¿Cuáles son las pautas actuales para la profilaxis de TEV después de un parto por cesárea? Varias pautas definen los factores de riesgo de TEV, incluidos los resumidos en la Tabla 1 del Colegio Estadounidense de Médicos del Pecho (ACCP), el Real Colegio de Obstetras y Ginecólogos (RCOG) y la Asociación Nacional para la Seguridad Materna (NPMS).
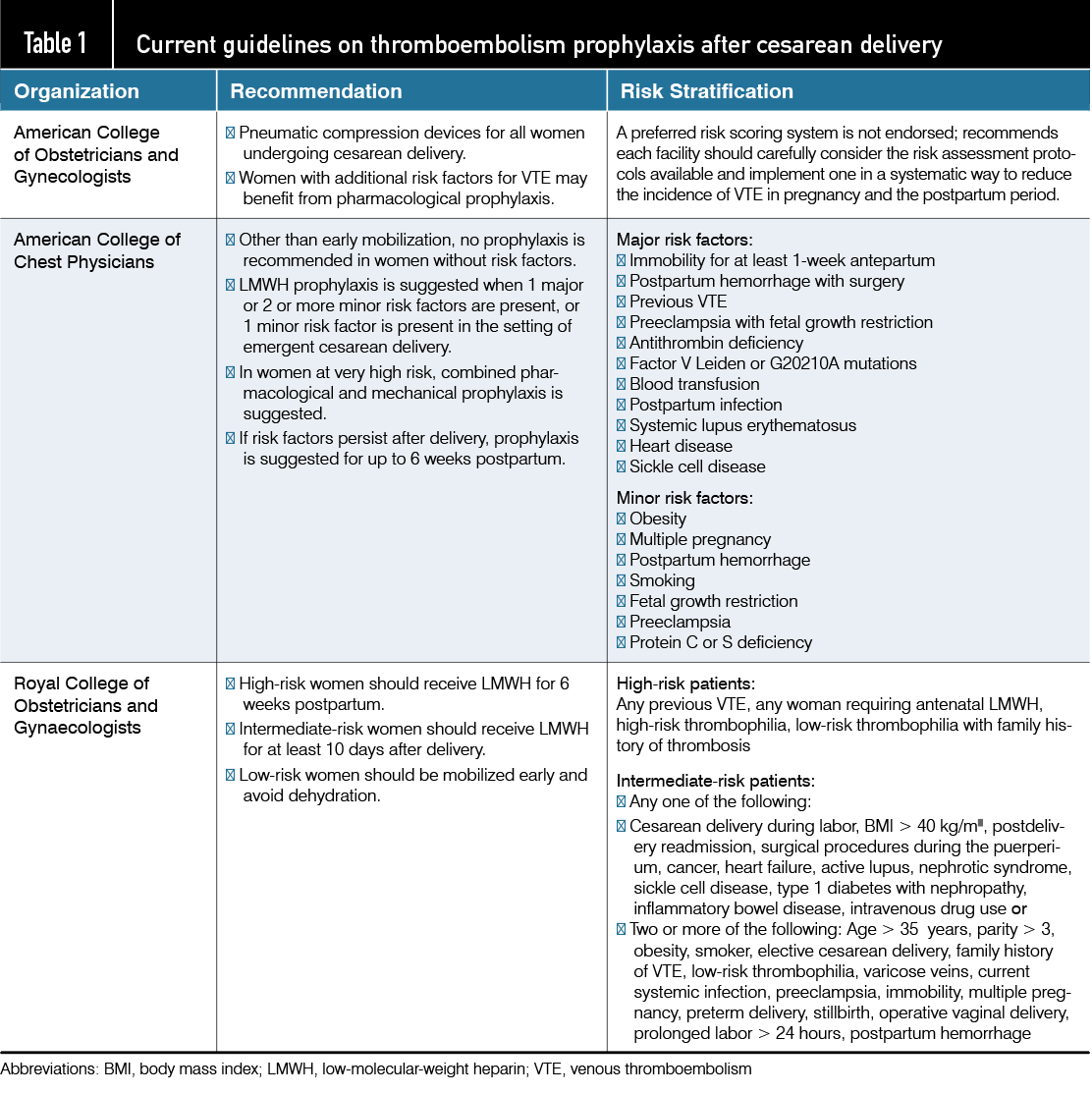
El Colegio Estadounidense de Obstetras y Ginecólogos (ACOG) recomienda que todas las mujeres que se someten a un parto por cesárea reciban profilaxis mecánica con el uso de dispositivos de compresión neumática secuencial que se inician antes de la operación y continúan hasta que la paciente puede caminar.
El uso de profilaxis farmacológica y mecánica combinada también puede respaldarse en función de la evaluación de riesgos individual. ACOG no respalda ninguna guía específica de estratificación de riesgo. Se anima a los hospitales a evaluar a las mujeres en busca de factores de riesgo de TEV y a implementar un protocolo de profilaxis que sopese los beneficios, los daños y la rentabilidad. Si los factores de riesgo de TEV persisten durante el período posparto, se debe considerar hasta 6 semanas de profilaxis farmacológica.
La ACCP sugiere que los beneficios de la tromboprofilaxis superan el daño potencial cuando el riesgo absoluto de TEV es del 3% o más. La presencia de 1 factor de riesgo mayor, 1 factor de riesgo menor en el contexto de un parto por cesárea de emergencia o 2 o más factores de riesgo menores sugiere un riesgo de TEV superior al 3%.
Para las mujeres que se someten a cesárea sin factores de riesgo de TEV, la ACCP no recomienda ninguna profilaxis que no sea la movilización temprana.
En mujeres con muy alto riesgo de TEV, se sugiere la profilaxis farmacológica y mecánica combinada. Si los factores de riesgo de TEV persisten durante el período posparto, se sugiere hasta 6 semanas de profilaxis.
El RCOG recomienda la tromboprofilaxis con heparina de bajo peso molecular (HBPM) durante 10 días después del parto para todas las mujeres que han tenido cesáreas y aquellas que tienen una cesárea electiva que tienen factores de riesgo adicionales. Se recomienda la profilaxis con HBPM durante 10 días después del parto en mujeres de riesgo intermedio y durante al menos 6 semanas después del parto en mujeres de alto riesgo.
El NPMS recomienda dispositivos de compresión neumática universales para todas las mujeres que se someten a cesáreas.
Se puede considerar la adición de profilaxis farmacológica para mujeres con alto riesgo de TEV según el uso de las pautas del RCOG o del sistema de puntuación Caprini modificado. Los hospitales pueden considerar la posibilidad de proporcionar profilaxis farmacológica para la TEV a todas las mujeres que se someten a una cesárea debido a los desafíos para identificar sistemáticamente a las mujeres con factores de riesgo de TEV.
¿Existe evidencia suficiente para recomendar una guía específica sobre la otra? En general, todas las mujeres con un episodio previo de TEV requieren dosis profilácticas de LMWH o heparina no fraccionada (UFH) durante al menos 6 semanas después del parto. Mujeres sin antecedentes personales de TEV pero que han dado positivo en una de las trombofilias hereditarias de alto riesgo (deficiencia de antitrombina III, factor V Leiden homocigoto o G20210A, o heterocigotos tanto para el factor V Leiden como para el G20210A) o que tienen un bajo trombofilia de riesgo también debe recibir profilaxis farmacológica de TEV después de un parto por cesárea.
Las mujeres con un diagnóstico previo de síndrome de anticuerpos antifosfolípidos deben recibir dosis profilácticas o terapéuticas de heparina (según la historia previa de TEV) durante el puerperio, independientemente del modo de parto.
La principal discrepancia entre las guías actuales se refiere a la profilaxis farmacológica para mujeres sin antecedentes de TEV y sin trombofilia hereditaria o adquirida. Las recomendaciones difieren en parte porque se basan en estudios observacionales y opiniones de expertos debido a la falta de datos de ensayos clínicos.
Esto presenta un desafío para determinar la verdadera incidencia de TEV y evaluar con precisión la relación riesgo-beneficio de la profilaxis farmacológica después de la cesárea. El beneficio potencial de la profilaxis farmacológica debe sopesarse con el potencial de resultados adversos asociados con la intervención.
Por ejemplo, el uso de profilaxis farmacológica de TEV después de una cesárea se ha asociado con mayores tasas de separación de heridas y hematomas de heridas. En ausencia de ensayos clínicos con el poder estadístico adecuado, los cálculos precisos del número necesario a tratar (NNT) y el número necesario para dañar (NND) son limitados. Sin embargo, la evidencia disponible sugiere que el NNH puede ser menor que el NNT en la mayoría de los escenarios, particularmente en ausencia de factores de riesgo o en presencia de solo un factor de riesgo menor.
Además, los datos administrativos y retrospectivos obtenidos del análisis de grandes bases de datos pueden sobrestimar la incidencia de TEV, lo que resulta en una sobrestimación similar del beneficio de cualquier intervención destinada a prevenirlo.
Otra consideración al hacer recomendaciones es que el uso de modelos de evaluación de riesgos (p. Ej., Caprini y Padua) para predecir el TEV después de una cesárea no se ha estudiado de manera adecuada.
Los autores de un estudio reciente que cuestiona su utilidad durante el período periparto sugieren el establecimiento de un registro clínico materno y una investigación más extensa para identificar modelos óptimos con los que predecir el riesgo de TEV en la población obstétrica.
En la actualidad, la evidencia disponible que sugiere que la profilaxis farmacológica universal (o casi universal) de TEV reduce efectivamente la mortalidad materna es limitada. Cualquier beneficio atribuible de la profilaxis farmacológica universal de TEV después de una cesárea en la mortalidad materna probablemente será bajo debido a la rareza del evento.
Un estudio reciente informó sólo una muerte materna por TEV entre 465,880 mujeres sometidas a cesárea cuando todas las mujeres recibieron profilaxis mecánica (p. Ej., Dispositivos de compresión secuencial).
¿Qué agentes farmacológicos se utilizan habitualmente para la profilaxis del tromboembolismo venoso? Los dos agentes más comunes utilizados para la profilaxis de TEV son LMWH y UFH. Las guías actuales recomiendan la HBPM (p. Ej., Enoxaparina) como agente farmacológico de primera línea. No se recomienda enoxaparina en pacientes con disfunción renal significativa, definida como un aclaramiento de creatinina menor de 30 ml / min.
En comparación con la HNF, la enoxaparina tiene la ventaja de una mejor biodisponibilidad, una vida media más larga, un efecto de anticoagulación más predecible, menos riesgos de hemorragia y menos riesgo de trombocitopenia y osteopenia inducidas por heparina.
Para fines de profilaxis, la dosis recomendada de enoxaparina es típicamente de 40 mg por vía subcutánea una vez al día. Las mujeres obesas pueden requerir dosis más altas; sin embargo, se desconoce la dosis óptima. Alguna evidencia apoya el uso de dosis intermedias de enoxaparina (40 mg por vía subcutánea cada 12 horas) para mujeres obesas.
La HNF es una buena opción en mujeres con enfermedad renal. Las dosis profilácticas recomendadas oscilan entre 5000 y 10,000 unidades por vía subcutánea cada 12 horas dependiendo de la edad gestacional (5000 unidades por vía subcutánea cada 12 horas en el primer trimestre, 7500 unidades por vía subcutánea cada 12 horas en el segundo trimestre y 10,000 unidades por vía subcutánea cada 12 horas durante el tercer trimestre).
En el puerperio, se suelen utilizar dosis de 5000 unidades por vía subcutánea cada 8 a 12 h. No hay datos suficientes para recomendar el uso de nuevos anticoagulantes orales (p. Ej., Apixaban, rivaroxaban, dabigatrán) durante el período posparto.
¿Cuándo es el momento óptimo para iniciar la profilaxis de la tromboembolia después de una cesárea? Las pautas actuales del ACOG recomiendan comenzar la profilaxis mecánica de TEV con dispositivos de compresión secuencial antes de la operación en todas las mujeres que se someten a una cesárea.
La Society for Obstetric Anesthesia and Perinatology (SOAP) ha abordado el intervalo óptimo entre la anestesia neuroaxial y el inicio de la profilaxis farmacológica de TEV para prevenir el desarrollo de hematomas espinales o epidurales. Las dosis profilácticas de enoxaparina (40 mg por vía subcutánea todos los días) pueden iniciarse en el posoperatorio tan pronto como 4 horas después de la extracción del catéter, pero no antes de las 12 horas posteriores a la realización del bloqueo. También se pueden iniciar dosis intermedias de enoxaparina (40 mg por vía subcutánea cada 12 horas) y dosis terapéuticas tan pronto como 4 horas después de la extracción del catéter, pero no antes de las 24 horas posteriores a la realización del bloqueo. Las dosis profilácticas de UFH se pueden iniciar tan pronto como 1 hora después de la extracción del catéter neuroaxial.
Además de las preocupaciones sobre los hematomas espinales, el momento para iniciar la profilaxis de TEV también debe considerar el riesgo de hemorragia posoperatoria.
Con dosis profilácticas de anticoagulación, las complicaciones hemorrágicas suelen ser leves y rara vez provocan una hemorragia potencialmente mortal, a diferencia de los riesgos hemorrágicos con el uso de anticoagulación en dosis completa en el período posoperatorio.
En los casos con complicaciones hemorrágicas intraoperatorias importantes, la decisión de cuándo iniciar la profilaxis farmacológica (si está indicada) debe ser individualizada, reconociendo que la hemorragia posparto, la transfusión de sangre y la cirugía prolongada son factores de riesgo de TEV. En estos casos, puede ser prudente iniciar la HNF, que es reversible y tiene una vida media más corta.
Conclusión. La TEV sigue siendo una causa importante de morbilidad y mortalidad materna durante el embarazo y el período posparto.
El uso de dispositivos de compresión secuencial de profilaxis mecánica es una intervención económica y segura y debe usarse en todas las mujeres sometidas a cesárea hasta que la mujer sea completamente ambulatoria.
La decisión de añadir profilaxis farmacológica depende de la presencia o ausencia de determinados factores de riesgo. Las mujeres con antecedentes personales de trombosis venosa profunda o embolia pulmonar y las mujeres con antecedentes personales de trombofilia hereditaria deben recibir profilaxis farmacológica después de una cesárea.
El uso de profilaxis farmacológica universal o casi universal para mujeres sometidas a cesárea, que no sean aquellas con trombosis previa o trombofilia hereditaria, no puede recomendarse hasta que estudios adicionales demuestren que tal estrategia es beneficiosa.

No hay comentarios:
Publicar un comentario