El síndrome de ovario poliquístico (SOP) es una afección endocrina y metabólica que afecta hasta al 20 % de las mujeres premenopáusicas. Es multifactorial, con una etiología en gran parte desconocida. El síndrome se caracteriza por una tríada de hiperandrogenismo, disfunción ovulatoria y morfología de ovario poliquístico (PCOM).

La disfunción ovulatoria a menudo se presenta como amenorrea, ciclos menstruales irregulares (perdidos o retrasados) o infertilidad. En una mujer o adolescente a más de 3 años de la menarquia, los ciclos menstruales irregulares se definen como ciclos que duran menos de 21 días o más de 35 días, menos de 8 ciclos en total por año o más de 90 días para cualquier ciclo.
El PCOM se define como la presencia de folículos antrales mayores o iguales a 20 por ovario (antes 12) o un volumen mayor o igual a 10 mL por ovario, de acuerdo con las guías internacionales más recientes (Figura 2 ).
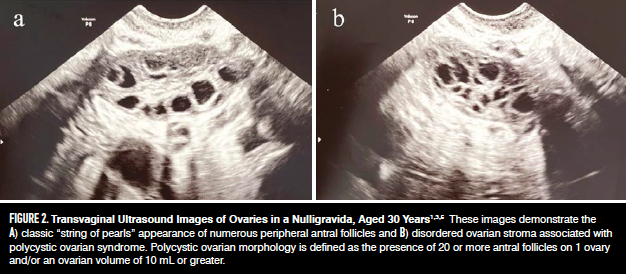
Las mujeres con SOP también corren el riesgo de sufrir secuelas de salud a largo plazo, como infertilidad, resistencia a la insulina, obesidad, enfermedades cardiovasculares, síndrome metabólico, apnea obstructiva del sueño y trastornos del estado de ánimo. Es crucial comprender los criterios de diagnóstico para diferenciar el SOP de otros diagnósticos de presentación similar. El manejo del SOP varía según la fase de la vida reproductiva de la mujer e incluye una combinación de modificaciones del estilo de vida y tratamientos farmacológicos dirigidos a síntomas específicos.
Diagnóstico. No existe una definición universalmente aceptada de PCOS. Una clasificación bien conocida son los criterios de Rotterdam de 2003, que ampliaron la definición de los Institutos Nacionales de Salud (NIH) de 1990. La definición de Rotterdam establece que se deben cumplir 2 de los siguientes 3 criterios para tener el síndrome: hiperandrogenismo (ya sea clínico o bioquímico), disfunción ovulatoria o PCOM. Como se mencionó, esto amplió los criterios del NIH de 1990, que definían el SOP como la presencia de disfunción ovulatoria con hiperandrogenismo y no incorporaban hallazgos ultrasonográficos en los criterios.
Los criterios de la Sociedad de exceso de andrógenos de 2006 requieren hiperandrogenismo junto con disfunción ovulatoria o PCOM para hacer el diagnóstico de SOP. La declaración de consenso de los NIH de 2012 clasifica además 4 fenotipos de SOP en función de los criterios utilizados para establecer el diagnóstico. Estos incluyen fenotipo A (hiperandrogenismo, disfunción ovulatoria y PCOM), fenotipo B (hiperandrogenismo y disfunción ovulatoria), fenotipo C (hiperandrogenismo y PCOM) y fenotipo D (disfunción ovulatoria y PCOM).
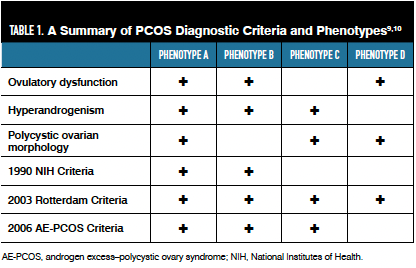
Las guías internacionales más recientes de 2018 respaldan el uso de los criterios de Rotterdam para establecer un diagnóstico de SOP en adultos. Cada uno de los criterios diagnósticos enfatiza la necesidad de descartar diagnósticos alternativos adicionales. Antes de establecer un diagnóstico de SOP, se deben tener en cuenta otras causas de irregularidades menstruales o hiperandrogenismo. Por ejemplo, la hiperplasia suprarrenal congénita no clásica debida a la deficiencia de 21-hidroxilasa también puede provocar hirsutismo, anomalías menstruales, hiperandrogenismo y ovarios poliquísticos. Las anomalías de la tiroides o los niveles elevados de prolactina sérica pueden provocar ciclos menstruales irregulares. Los tumores suprarrenales secretores de andrógenos pueden causar hirsutismo y/o hiperandrogenismo. En comparación con el síndrome de ovario poliquístico, estas neoplasias se presentan con elevaciones más extremas de los andrógenos séricos o un inicio más agudo de los síntomas del hirsutismo.
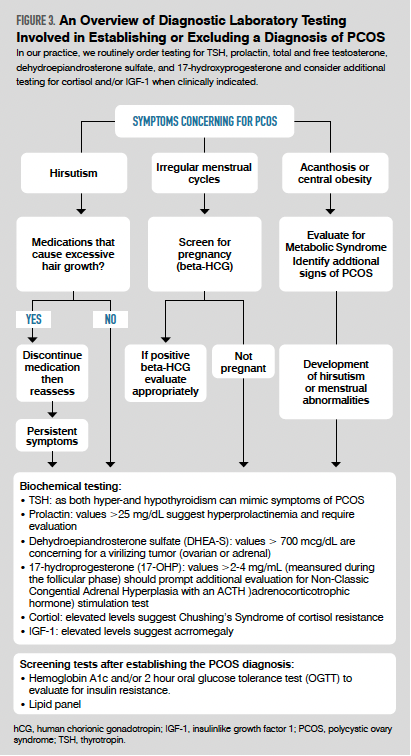
Patogenia del SOP. La patogenia del SOP es multifactorial y un área activa de investigación en curso. Los estudios de gemelos sugirieron inicialmente una base genética para el SOP. Más recientemente, los estudios de asociación de todo el genoma han identificado 19 loci específicos asociados con PCOS, la mayoría de los cuales se comparten entre mujeres de diferentes razas. Sin embargo, estos 19 loci genéticos representan menos del 10 % de la heredabilidad del SOP, lo que sugiere el papel de los factores ambientales. El impacto del medio ambiente en el SOP en un individuo genéticamente predispuesto puede comenzar en el útero y continuar durante toda la vida del individuo, con influencias ambientales que incluyen la geografía, la nutrición, el estado socioeconómico y la exposición a toxinas. dieciséis
Aunque no existe una “dieta de SOP” específica para los pacientes, las investigaciones han demostrado que el almidón, el suero de leche y los productos lácteos tienen efectos negativos en la función metabólica de las mujeres con SOP y que las frutas y los frijoles (alimentos ricos en inositol) tienen un efecto positivo. Además, las mujeres con SOP y deficiencia de vitamina D tienen un mayor riesgo de disglucemia.
El impacto del estatus socioeconómico en el SOP se examinó en un estudio de 2011, que encontró que las mujeres con un nivel educativo alto cuyos padres tenían un nivel educativo bajo (definido como inferior a la escuela secundaria) tenían el mayor riesgo de desarrollar SOP, después de ajustar por edad, índice de masa corporal (IMC) y raza (odds ratio ajustado, 2,5; IC del 95 %, 1,4-4,4).
También existe una asociación negativa entre las sustancias químicas disruptoras endocrinas y el síndrome de ovario poliquístico. Un ejemplo de ello es el bisfenol A (BPA), un compuesto que se encuentra en los productos plásticos de consumo y que puede precipitar un ciclo de retroalimentación negativa. Un nivel elevado de BPA en suero puede conducir a niveles elevados de andrógenos, que luego afectan el metabolismo de BPA, aumentando aún más los andrógenos en suero circulantes.
Los fenotipos de PCOS difieren en mujeres de varias razas y etnias en los Estados Unidos e internacionalmente. Por ejemplo, el hirsutismo es más frecuente y/o grave en las mujeres del Medio Oriente, el Mediterráneo, la India y el sur de Asia que en las mujeres del este de Asia o blancas de los EE. UU. Con base en estos hallazgos, algunos han sugerido definiciones raciales y étnicas específicas del hirsutismo. Las diferencias raciales/étnicas en el hirsutismo pueden estar relacionadas con factores ambientales, como se analiza a continuación, o factores genéticos, como la herencia o la expresión. de 5α reductasa, una enzima que convierte la testosterona en dihidrotestosterona, un andrógeno más potente.
Consecuencias metabólicas del SOP y pautas de detección. Las personas con SOP también corren el riesgo de sufrir secuelas de salud perjudiciales a largo plazo. La resistencia a la insulina (RI) es uno de los riesgos más notables asociados con el síndrome de ovario poliquístico, y un metanálisis reciente encontró una razón de probabilidad de 3,26 (IC del 95 %: 2,17 a 4,90) en comparación con la población general. En mujeres con SOP, la RI se ha asociado con una mayor prevalencia de intolerancia a la glucosa de aparición temprana (30 %-40 %) y diabetes tipo 2 (10 %), y este riesgo es independiente de la presencia de obesidad. Los pacientes con SOP deben someterse a una prueba de detección IR en el momento del diagnóstico de SOP y cada 1 a 3 años a partir de entonces. 3,5,29Se puede usar una prueba de tolerancia oral a la glucosa (OGTT), la glucosa plasmática en ayunas o la hemoglobina A1C para evaluar el estado glucémico, pero se recomienda una OGTT en mujeres de alto riesgo (es decir, IMC > 25 kg/m2 o > 23 kg/m2 en Mujer asiática). En pacientes que deseen quedar embarazadas, se debe ofrecer la SOG de 75 g antes de la concepción, y si una mujer ya está embarazada, la prueba debe completarse antes de las 20 semanas de gestación debido al riesgo elevado de diabetes gestacional.
La obesidad está muy asociada con el SOP e intensifica las características del SOP, como la infertilidad y la IR. La obesidad por sí sola es un factor de riesgo para el desarrollo de la apnea obstructiva del sueño (AOS), pero investigaciones recientes reconocen una asociación entre la obesidad y el síndrome de ovario poliquístico. Se ha encontrado que las tasas de AOS son de 5 a 10 veces más altas en pacientes obesas y con SOP.30 La AOS aumenta el riesgo de que una mujer con SOP desarrolle una enfermedad cardiovascular (ECV).
La dislipidemia es otro efecto adverso clave del SOP, con una prevalencia de hasta el 70 %. La Androgen Excess Society recomienda que todas las pacientes con SOP se realicen un panel de lípidos en ayunas completo como herramienta de detección. El SOP, en mujeres con obesidad y sin ella, está asociado con niveles elevados de colesterol total y lipoproteínas de baja densidad, lo que pone a las pacientes en riesgo de síndrome metabólico y ECV.
La asociación entre PCOS y CVD no es concluyente, pero la investigación ha demostrado una correlación entre la exposición a lo largo del tiempo y el empeoramiento de la enfermedad en esta población. Se ha demostrado que existe un aumento de la calcificación de la arteria coronaria y la aorta en pacientes con SOPQ que empeora con la edad, lo que lleva a la aterosclerosis prematura o enfermedad vascular subclínica. Las pautas de detección recomendadas para ECV en mujeres con SOP incluyen una medición del peso y el IMC cada 6 a 12 meses y una medición de la presión arterial al menos una vez al año. Las mujeres con síndrome de ovario poliquístico deben considerarse en riesgo de ECV si tienen factores de riesgo adicionales (obesidad, tabaquismo, dislipidemia, hipertensión, intolerancia a la glucosa o falta de actividad física).
La hiperplasia endometrial es otra secuela del síndrome de ovario poliquístico y un factor de riesgo para el desarrollo de carcinoma endometrial. Esto se debe en gran parte a la exposición al estrógeno no suprimida relacionada con estados anovulatorios en el SOP. Las mujeres con SOP tienen al menos 3 veces más probabilidades de desarrollar cáncer de endometrio que las mujeres sin SOP. No se recomienda la detección sistemática de cáncer de endometrio; sin embargo, los proveedores deben tener un umbral bajo para la evaluación de amenorrea o sangrado vaginal anormal en mujeres con SOP y considerar una ecografía o una biopsia endometrial. No existen recomendaciones oficiales para la prevención óptima de la hiperplasia endometrial; sin embargo, las pautas internacionales de 2018 sugieren el tratamiento con píldoras anticonceptivas orales combinadas o progesterona si los ciclos duran más de 90 días.
PCOS también está asociado con trastornos de salud mental que a menudo no están representados. Aproximadamente el 40 % de las mujeres con SOP, en particular las más jóvenes, experimentan depresión. Debido a la alta prevalencia, todas las mujeres con SOP deben someterse a pruebas de detección de ansiedad y depresión en el momento del diagnóstico y de forma rutinaria a partir de entonces. apariencia. Los médicos también deben ser conscientes de la mayor prevalencia de trastornos de la alimentación en mujeres con SOP y, si se sospecha, las pacientes deben ser examinadas y derivadas de manera adecuada a especialistas.
Modificaciones de estilo de vida. Para reducir el riesgo de consecuencias metabólicas, se debe asesorar a las pacientes con SOP sobre modificaciones en el estilo de vida, incluida la nutrición, el ejercicio y las estrategias conductuales. La recomendación general es para comidas saludables y bien balanceadas. En mujeres con SOP que buscan perder peso, puede ser eficaz reducir la ingesta calórica hasta en un 30% (500-700 cal/d). También se debe aconsejar a los pacientes sobre la importancia del ejercicio constante de intensidad media o alta (al menos 75-150 min/semana), incluido el entrenamiento de fuerza, y reducir las actividades sedentarias. Las estrategias conductuales de establecimiento de metas y autocontrol pueden ser útiles en el control del peso y el bienestar general en mujeres con SOP. En mujeres con SOP que tienen sobrepeso u obesidad, incluso una pérdida de peso del 5% al 10% mejora significativamente los resultados metabólicos y de fertilidad.
Tratamientos farmacológicos. Varios tratamientos farmacológicos se enfocan en los síntomas específicos del síndrome de ovario poliquístico, particularmente los ciclos menstruales irregulares y los síntomas de hiperandrógenos. Los anticonceptivos hormonales combinados (CHC, píldoras, anillos vaginales y parches) se consideran de primera línea. No existe una formulación o dosis específica de estrógeno o progesterona en AHC que se prefiera, por lo que los médicos deben seguir las pautas estándar para las contraindicaciones de AHC. A las mujeres con anovulación u oligoovulación que no son candidatas para AHC se les debe ofrecer otras formas de progestágenos para prevenir la hiperplasia endometrial y la malignidad. Estas opciones incluyen formas locales de progesterona (es decir, un dispositivo intrauterino de levonorgestrel para mantener un revestimiento endometrial delgado) o progesterona oral cíclica. Se pueden considerar los antiandrógenos (como la espironolactona oral) si los síntomas del hirsutismo no mejoran con 6 meses de uso de AHC o si el paciente tiene contraindicaciones para los AHC.
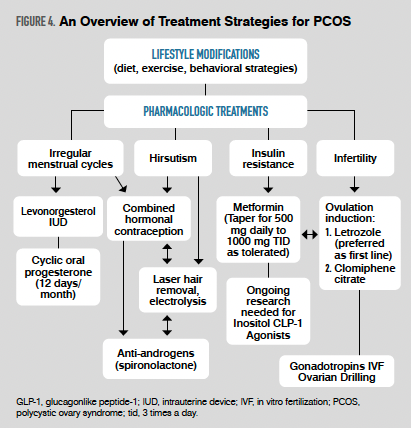
Las mujeres con SOP en riesgo de desarrollar RI deben recibir asesoramiento sobre modificaciones en el estilo de vida, pero también deben ser consideradas candidatas para metformina. La metformina generalmente se inicia con una dosis baja (500 mg al día) y se aumenta gradualmente hasta 1000 mg 3 veces al día durante varias semanas. El inositol es un azúcar natural que se ha demostrado que mejora la sensibilidad a la insulina y, aunque hay pruebas emergentes de su uso en mujeres con SOP e RI, todavía se considera experimental.
Por último, los agonistas del péptido 1 similar al glucagón (GLP-1) se han vuelto cada vez más populares para promover la pérdida de peso al retrasar el vaciado gástrico e inhibir el apetito. Un metanálisis de 2019 encontró que los agonistas de GLP-1 fueron más efectivos que la metformina para mejorar la sensibilidad a la insulina y reducir la circunferencia abdominal y el IMC en mujeres con SOP. Aunque estos fueron hallazgos emocionantes, los autores de este metanálisis concluyeron que la evidencia disponible es de calidad moderada a baja y que se necesitan estudios adicionales de mayor calidad para determinar la seguridad y eficacia de los agonistas de GLP-1 en el manejo del SOP. Las pautas actuales establecen que los medicamentos contra la obesidad (como los agonistas de GLP-1) deben considerarse experimentales para su uso en el síndrome de ovario poliquístico.
El manejo de la infertilidad para el SOP se enfoca en la inducción de la ovulación. El letrozol y el citrato de clomifeno son medicamentos orales que se usan en combinación con relaciones sexuales programadas o inseminación intrauterina para lograr el embarazo. Un estudio histórico encontró que las mujeres con SOP que recibieron letrozol tenían tasas de nacidos vivos acumuladas más altas que el grupo de clomifeno, sin diferencias significativas en gestaciones multifetales, anomalías fetales congénitas o pérdidas de embarazo. En los casos en que el letrozol no esté disponible o la paciente tenga una respuesta deficiente al medicamento, se puede usar citrato de clomifeno para inducir la ovulación. Si factores adicionales contribuyen a la infertilidad de la pareja, puede ser apropiado derivarlos a un endocrinólogo reproductivo para el uso potencial de gonadotropinas y/o fertilización in vitro.
Conclusiones. El SOP es un trastorno endocrino común que afecta a las mujeres en edad reproductiva. Es importante comprender los criterios de diagnóstico para diferenciar esta afección de otros diagnósticos de presentación similar. Varias consecuencias están asociadas con el SOP, que incluyen infertilidad, resistencia a la insulina, dislipidemia, síndrome metabólico, OSA y trastornos del estado de ánimo, que deben considerarse y detectarse adecuadamente.
El manejo del SOP incluye una combinación de modificaciones en el estilo de vida y tratamientos farmacológicos dirigidos a síntomas específicos. Los anticonceptivos hormonales combinados son el tratamiento de primera línea para el hirsutismo y los ciclos menstruales irregulares, y el letrozol es el tratamiento de primera línea para la infertilidad anovulatoria/oligoovulatoria asociada con el síndrome de ovario poliquístico.

No hay comentarios:
Publicar un comentario