La decidualización es un proceso básico de transformación de hESC que limita el impacto de la invasión de trofoblasto. Los defectos en este proceso dan lugar a resultados adversos del embarazo.
Nuestra investigación previa demostró una decidualización aberrante que contribuye a las alteraciones fenotípicas asociadas con la sPE.
El perfil transcripcional ha revelado defectos en la expresión génica durante la decidualización in vitro de hESCs de pacientes anteriores con sPE. Entre los múltiples genes desregulados, se encontró que ANXA2 estaba regulado negativamente en hESCs decidualizadas de mujeres con SPE previo en comparación con mujeres con embarazos previos normales.
Debido a que ANXA2 es un biomarcador de la biología endometrial y la decidualización encontrada en nuestro trabajo anterior, el presente estudio se centró en su implicación en la resistencia a la decidualización asociada con el sPE. Utilizando nuestros modelos in vitro e in vivo de silenciamiento de ANXA2 , demostramos la relevancia de este biomarcador endometrial que regula la decidualización y la placentación y cómo su deficiencia puede explicar, al menos en parte, la invasión uterina superficial por trofoblasto placentario en sPE. Nuestros hallazgos resaltan la contribución materna a la patogénesis de sPE y sugieren que la evaluación de ANXA2 puede ayudar al desarrollo de terapias enfocadas en mejorar la decidualización y prevenir esta enfermedad.
Los experimentos de decidualización in vitro demostraron que las hESC de mujeres con sPE previa habían reducido significativamente la expresión de ANXA2 en comparación con las hESCs de control, corroborando nuestros datos transcriptómicos anteriores. Debido a que el papel de ANXA2 en el proceso de decidualización era desconocido anteriormente, utilizamos siRNA para bloquear la expresión génica y demostramos un defecto de decidualización de hESCs empobrecidos por ANXA2.
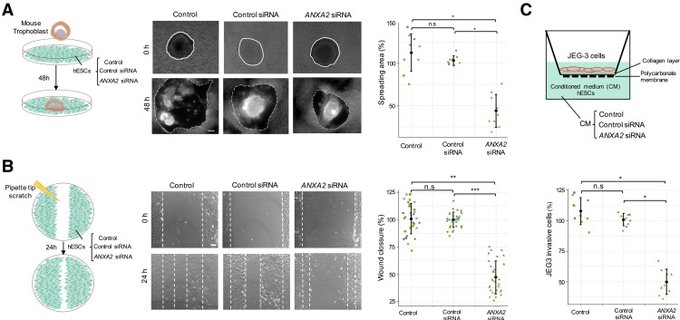
La evidencia de la decidualización aberrante incluyó la prevención de la polimerización de filamentos de actina, con una fracción filamentosa de actina F disminuida y la falta de secreción de los biomarcadores de decidualización clásicos prolactina e IGFBP1. ROCK, una proteína que interactúa con ANXA2 durante el reordenamiento del citoesqueleto, es una molécula clave de señalización intracelular que coordina la propagación celular, la motilidad y el cambio de forma.
Al igual que el agotamiento de ANXA2 , la inactivación de la proteína ROCK se asoció con defectos de decidualización in vitro, lo que sugiere una vía común. En la decidualización normal, los hESC aumentan su capacidad de ser invadidos por el trofoctodermo durante los eventos iniciales de implantación. En presencia de células del trofoblasto, las células del estroma decidual adquieren una mayor motilidad y migran lejos del sitio de implantación.
Aquí, demostramos que el silenciamiento de ANXA2 no afecta la unión del embrión sino que interfiere con la motilidad de hESC y la propagación e invasión de trofoblasto, lo que muestra una capacidad reducida para acomodar el trofoblasto invasor. Este hallazgo sugiere un mecanismo en el que ANXA2 y ROCK regulan la decidualización y la posterior motilidad del estroma, la migración y la reorganización del citoesqueleto, asegurando la invasión regulada de los blastocistos.
Nuestros datos abordan el papel de ANXA2 en la decidualización y el desarrollo placentario in vivo. Aunque las hembras Anxa2 - / - ratones son fértiles, manifiestan un defecto de decidualización in vivo. Nuestro hallazgo de que los marcadores de prolactina e IGFBP1 se reducen notablemente en los tejidos deciduales en ratones Anxa2 - / - se correlaciona con nuestros hallazgos in vitro con hESC decidualizados de individuos con sPE previo.
Curiosamente, mientras que los ratones Anxa2 - / - tienen tamaños de camada normales, la evaluación de la masa corporal en parejas de camadas alimentadas ad libitum de 2 a 12 meses de edad revela una reducción de peso de 10 a 13%.
Este hallazgo concuerda con nuestros datos que indican que, aunque el número de sitios de implantación es similar entre los ratones Anxa2 - / - y Anxa2 + / + , hay un peso reducido en el sitio de implantación, peso fetal y masa placentaria durante la gestación. Este hallazgo demuestra que la ausencia de ANXA2 está asociada con la restricción del crecimiento intrauterino y la función placentaria deteriorada, y sugiere además que podría tener un papel etiológico en los hESC decidualizados humanos en la sPE, en la que la expresión de ANXA2 a menudo se reduce. De manera similar, los ratones nulos Anxa2 - / - exhiben daño placentario y desarrollo vascular deteriorado, como lo demuestra la tinción para CD31 y vWF. CD31 es un marcador endotelial involucrado en la angiogénesis, y su falta de expresión en decidua y placenta se asocia con preeclampsia.
VWF tiene un papel central en la hemostasia primaria, y sus niveles también se correlacionan con el riesgo de trombosis y se correlacionan inversamente con el riesgo de sangrado dentro de una población aparentemente sana. Ambos marcadores parecen reducirse significativamente en los tejidos uterinos de ratones Anxa2 - / - , lo que sugiere que la vascularización y la hemostasia en la interfaz materno-fetal es defectuosa, lo cual es una característica básica de la preeclampsia.
Tomados en conjunto, estos datos indican que los mecanismos in vivo que regulan la decidualización se ven afectados en ausencia de ANXA2 , lo que respalda un papel importante para ANXA2 en la decidualización y el desarrollo placentario.
La patogenia de la preeclampsia sigue siendo esquiva, y solo se sugiere que la dosis baja de aspirina sea efectiva para prevenir la preeclampsia prematura en subgrupos de mujeres según su historial médico y obstétrico.
El ensayo ASPRE (Prueba combinada de detección de múltiples marcadores y tratamiento aleatorio de pacientes con aspirina para la prevención de la preeclampsia basada en la evidencia) demostró que las mujeres de alto riesgo que fueron identificadas por la prueba combinada de detección del primer trimestre que utilizaron biomarcadores para apuntar a pacientes de alto riesgo y fueron asignadas al azar para recibir aspirina (150 mg por noche) desde las 11-14 hasta las 36 semanas de gestación había reducido sustancialmente las tasas de preeclampsia prematura en comparación con las mujeres que recibieron placebo (aspirina: 1.6% versus placebo: 4.3%).
La atención preconcepcional tiene como objetivo optimizar los resultados reproductivos antes del embarazo. Nuestros resultados sugieren un nuevo vínculo mecanicista entre la deficiencia de ANXA2 y la decidualización defectuosa, lo que podría explicar cómo el entorno materno reduce la invasión decidual por las células del trofoblasto que inducen complicaciones de embarazo de inicio tardío como la preeclampsia. Estos resultados pueden proporcionar nuevas oportunidades para el diagnóstico basado en ANXA2 como biomarcador, como medir esta molécula en hESC que fueron inducidas a decidualizarse in vitro o secretadas al fluido endometrial. Esta simple prueba podría permitir la evaluación del riesgo de desarrollar SPE antes de la concepción, abriendo posibilidades para desarrollar nuevas intervenciones terapéuticas enfocadas en mejorar la decidualización.
Proponemos un modelo de resistencia a la decidualización en pacientes con SPE basado en la deficiencia de ANXA2 que puede ser útil para investigar la contribución materna a otras complicaciones del embarazo, como el aborto espontáneo recurrente o el parto prematuro. Demostramos que ANXA2 realiza una función importante aguas arriba de la vía ANXA2 / ROCK en la regulación de la remodelación de actina F, que impide la remodelación morfológica de hESCs durante la decidualización. Además, pérdida de ANXA2en hESCs inhibe las secreciones de prolactina e IGFBP1, los principales marcadores de decidualización.
Tomados en conjunto, los defectos en el reordenamiento del citoesqueleto y la falta de secreción durante la decidualización promueven un microambiente uterino defectuoso que podría conducir a una invasión trofoblasto superficial mientras se establece la interfaz materno-fetal durante la placentación. Los datos del modelo de ratón corroboran estos hallazgos in vivo y muestran que los mecanismos que regulan la decidualización se ven afectados en ausencia de ANXA2 , lo que respalda un papel importante para ANXA2 en la decidualización y el desarrollo placentario.
Abordamos in vitro e in vivo la prueba de concepto de que la deficiencia materna de ANXA2 podría ser un biomarcador potencial para la invasión decidual superficial por citotrofoblastos placentarios que conduce a preeclampsia, con nuevas implicaciones diagnósticas y / o terapéuticas. Nuestros hallazgos se limitan al papel funcional de la vía ANXA2 / ROCK para regular la decidualización y la placentación. Sin embargo, la firma transcriptómica asociada con la resistencia a la decidualización puede incluir más vías que están implicadas en el fenotipo asociado con el sPE. Además, la contribución materna a la sPE puede extenderse más que un defecto de decidualización. Por lo tanto, son necesarias investigaciones adicionales del fenotipo de resistencia a la decidualización para comprender completamente la contribución materna a la sPE.
Juntos, nuestros resultados sugieren que la decidualización de hESCs está mediada, al menos en parte, por ANXA2 y que la deficiencia materna de ANXA2 contribuye a la invasión decidual superficial por trofoblastos placentarios. Nuestros hallazgos resaltan la contribución materna a la patogénesis de sPE y sugieren que la evaluación de ANXA2 materno puede proporcionar una herramienta para nuevas intervenciones diagnósticas y / o terapéuticas en sPE.

No hay comentarios:
Publicar un comentario